O Que é Ligação Iônica e Covalente?

A ligação iônica é uma força de atração entre íons, que são partículas com carga elétrica. Estes íons podem ser positivos ou negativos e se atraem mutuamente para formar um composto químico. Os Íons são formados quando os elétrons dos elementos se transferem entre eles, resultando em um Átomo carregado positivamente (cátion) e outro carregado negativamente (ânion). A ligação iônica geralmente acontece entre metais e não-metais.
A ligação covalente é uma força de atração muito diferente da ligação iônica. Nesta força, dois ou mais átomos compartilham elétrons para preencher suas camadas externas de valência, estabelecendo assim uma conexão estável entre os dois. Esta conexão pode ser encontrada principalmente nos compostos orgânicos, que consistem principalmente em carbono e hidrogênio ligados por meio desta força molecular fraca chamada ligações covalentes.
Como Funcionam as Ligações Iônicas e Covalentes?
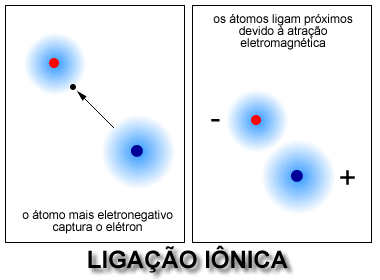
As ligações iônicas e covalentes são duas formas de ligação química que ocorrem entre átomos. A diferença entre elas é que as ligações iônicas se baseiam na transferência de elétrons, enquanto as covalentes envolvem a partilha de elétrons.
Ligações Iônicas: Ligações iônicas ocorrem quando um átomo doador (normalmente metal) transfere um ou mais pares de elétrons para outro átomo receptor (geralmente não-metal). Isso resulta em uma forte atração eletrostática entre os íons positivos e negativos, formando assim uma estrutura cristalina. As propriedades físicas desta estrutura dependem da natureza dos elementos envolvidos na reação, bem como da quantidade de carga total nos íons produzidos.
Ligações Covalentes: Ligações covalentes ocorrem quando dois átomos compartilham um par de elétrons para estabelecer sua ligação. O processo começa com os dois átomos contribuindo igualmente para a partilha dos pares eletrónicos; isso resultará numa molécula neutra porque ambos os lados têm a mesma quantidade de carga positiva e negativa. Esta união é geralmente muito fraca comparada às ligações iônicas, mas existem algumas excepções onde a força da ligação pode ser significativa devido à presença dos orbitais híbridizados no composto molecular resultante.
Quais São as Diferenças Entre Ligações Iônicas e Covalentes?
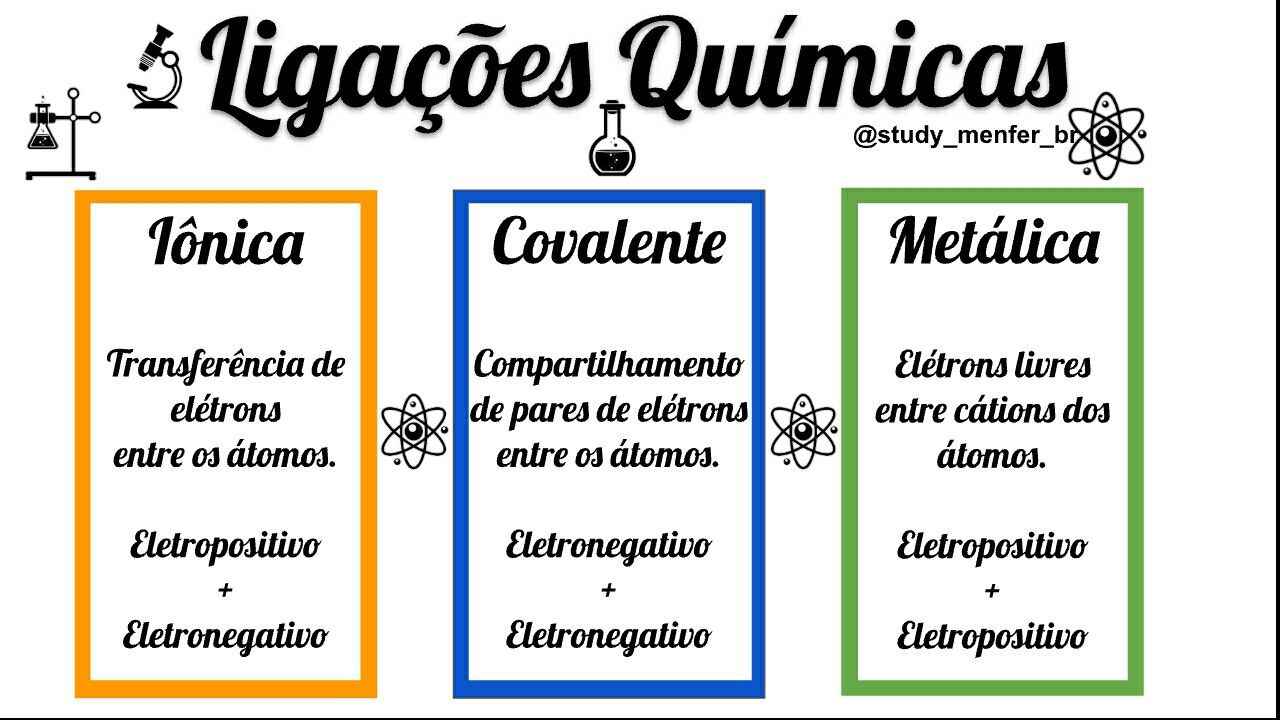
A principal diferença entre ligações iônicas e covalentes é a forma como os átomos se ligam. Em uma ligação iônica, um ou mais elétrons são transferidos de um átomo para outro, resultando em íons positivos e negativos que atraem uns aos outros. Já na ligação covalente, dois ou mais átomos compartilham elétrons para preencher suas camadas externas de valência. Isso geralmente acontece quando os elementos têm número iguais de elétrons disponíveis para compartilhar (isto é conhecido como “ligação molecular”). Outras diferenças incluem:
• Força da Ligação: A força da ligação iônica é maior do que a força da ligação covalente;
• Energia Envolvida: A energia envolvida na formação de uma ligação iônica é maior do que aquela necessária para formar uma ligação covalente;
• Polaridade: As moléculas ionizadas possuem polaridade enquanto as moléculas covalentes podem ser polares ou nãopolares;
• Solubilidade em Água: Compostos ionizados sólidos só se dissolvem facilmente em solventes polares como a água, enquanto compostoscovalentes solúveis dependem dos grupos funcionais presentes nas moléculas;
• Condutividade Elétrica: Os compostossolúveis condutores só podem ser obtidas por meio da dissociaçãode sais ionizados, enquanto no estado sólido.
Qual Tipo de Ligação É Mais Eficaz em Determinadas Situações?
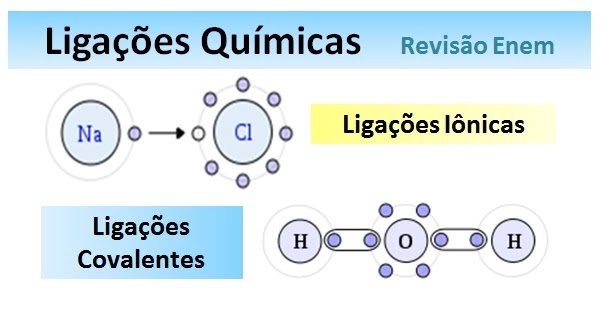
A resposta para essa pergunta depende da situação. As ligações iônicas são mais eficazes em determinadas situações, como na formação de sais iônicos ou na estabilização de estruturas cristalinas. Por outro lado, as ligações covalentes são mais eficazes quando se trata de estabilizar moléculas orgânicas complexas ou compartilhar elétrons entre átomos diferentes.
| Ligação Iônica | Ligação Covalente |
|---|---|
| Formada por troca de elétrons entre íons positivos e negativos. | Formada pela partilha de elétrons entre átomos neutros. |
| É mais fraca do que a ligação covalente. | É mais forte do que a ligação iônica. |
| Ocorre em sais minerais, como o cloreto de sódio (NaCl). | Ocorre em moléculas orgânicas, como o metano (CH4). |
O que é uma ligação iônica?
Uma ligação iônica é um tipo de ligação química entre íons (cargas positivas e negativas) que se atraem. Esta força de atração resulta na formação de moléculas ou cristais, dependendo da natureza dos íons envolvidos. Geralmente, as ligações iônicas são encontradas em sais minerais como o cloreto de sódio (NaCl).
Como a ligação covalente se diferencia da ligação iônica?
A ligação covalente se diferencia da ligação iônica porque a ligação covalente é formada quando dois átomos compartilham elétrons, enquanto que na ligação iônica os átomos trocam elétrons. Na ligação covalente, os átomos mantêm sua identidade eletrônica original, enquanto que na ligação iônica ocorre uma transferência de elétrons entre os átomos para formar um par de íons positivo e negativo.
Quais são os elementos envolvidos em uma ligação iônica?
Os elementos envolvidos em uma ligação iônica são íons. Os íons são partículas carregadas que se formam quando um ou mais elétrons são transferidos entre átomos, resultando na criação de dois novos íons com cargas opostas. Estes íons interagem entre si através da força eletrostática, formando assim a ligação iônica.
Qual é o processo de formação de uma ligação covalente?
O processo de formação de uma ligação covalente envolve a partilha de elétrons entre átomos. Quando dois átomos se aproximam, os níveis de energia dos elétrons mudam e as forças atrativas entre os átomos começam a trabalhar para uni-los. Os elétrons são compartilhados igualmente entre os dois átomos, resultando na formação da ligação covalente.
Quais são as principais propriedades das duas tipos de ligações químicas?
As principais propriedades das duas tipos de ligações químicas são:
– Ligação covalente: É uma ligação formada por compartilhamento de elétrons entre átomos. Esta ligação é responsável pela estabilidade dos compostos orgânicos e inorgânicos.
– Ligação iônica: É uma ligação formada pelo transferência de elétrons entre átomos, resultando em um par iônico (cátion + ânion). Esta ligação é responsável pela estabilidade dos sais minerais e outros compostos inorgânicos.
Que fatores influenciam na força e estabilidade dessas duas formas de ligar átomos entre si?
Os fatores que influenciam na força e estabilidade das ligações químicas entre átomos são: a distância de separação entre os átomos, o número de elétrons compartilhados, a energia envolvida na transferência dos elétrons, as cargas elétricas envolvidas e a presença de outras moléculas no ambiente.
Em que condições as moléculas comuns podem mudar sua estrutura, passando por transformações químicas para outras espécies moleculares mais estáveis?
As moléculas comuns podem mudar sua estrutura, passando por transformações químicas para outras espécies moleculares mais estáveis, quando são expostas a temperaturas elevadas ou à presença de catalisadores. Estes processos podem resultar na formação de novas ligações entre átomos e/ou na ruptura das ligações existentes.
Existem outros tipos de interações além desses dois tipos principais (ligações iônicas e covalentes)?
Sim, existem outros tipos de interações além das ligações iônicas e covalentes. Esses incluem ligações metálicas, pontes de hidrogênio, forças de van der Waals e dipolo-dipolo.

Comentários